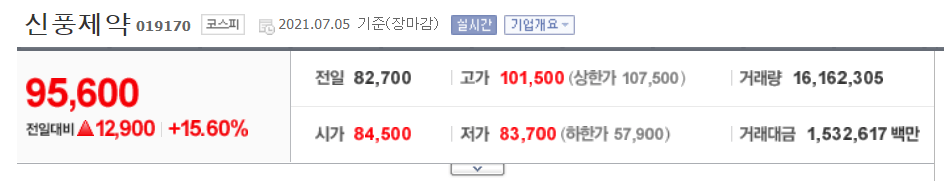
신풍제약이 강세다. 류머티즘과 약·항말라리아제 치료제가 코로나19 억제에 효능이 있다는 소식이 영향을 끼친 것으로 보인다. 신풍제약은 5일 오전 10시 16분 기준 전 거래일 대비 5.80%(4800원) 오른 8만 7500원에 거래됐다.

신풍제약은 코로나19 치료제로 개발 중인 '피라맥스'의 국내 임상 2상 시험 결과, 주평가지표에서 통계적 유의성을 확보하지 못했다고 오늘(5일) 밝혔습니다. 신풍제약의 코로나19(COVID-19) 치료제 '피라맥스(피로나리딘인산염과 알테수네이트복합제)'가 국내 임상시험 2상에서 일차 평가변수(주평 가지 표) 목표치를 달성하지 못했다.
국내 13개 대학병원서 113명 대상 임상결과
최근 의학계에 따르면 한남식 영국 케임브리지대 교수팀은 미국 식품의약국(FDA) 승인을 받은 의약품 성분 1917개를 인공지능(AI)으로 분석해 이 중 코로나19 치료제로 활용 가능한 약물 2개를 선정했다. 이 연구 결과를 국제학술지 ‘사이언스 어드밴시스’ 6월호에 발표했다.
2개 물질은 류머티즘 치료제로 쓰는 ‘설파살라진’과 말라리아 치료제로 사용하는 ‘프로구아닐’이다.신풍제약은 코로나19 바이러스 음성으로 전환된 환자의 비율(음전율)을 일차 평가변수로 정했는데, 피라맥스 투여군과 위약(가짜)군 간의 음전율에는 차이가 없다는 결과가 나왔다.

신풍제약은 5일 국내 2상 주요 결과(톱라인)를 발표
피라맥스는 피로나리딘인산염과 알테수네이트 복합제로, 항말라리아 치료제로 쓰던 의약품으로 신풍제약에서 코로나19 치료제로 개발하기 위한 임상시험을 해왔습니다. 이날 발표된 피라맥스의 임상 2상 시험은 13개 대학병원에서 총 113명의 경증 및 중등증 코로나19 환자를 대상으로 약물의 유효성과 안전성을 확인하고자 시행한 결과입니다.
신풍제약은 투여군과 대조군(위약군)으로 나눠 투여 후 28일까지 효과를 관찰했습니다. 신풍제약은 RT-PCR(실시간 유전자 증폭) 진단 검사를 했을 때 음성으로 전환되는 환자 비율(음전율)을 일차 평가변수로 잡았습니다. 그 결과 피라맥스 투여군 52명과 위약군 58명 간 차이가 없었습니다.

신풍제약 관계자는 "RT-PCR 기반 음성 기준값은 논란이 있고, 위양성(가짜양성) 문제가 제기되고 있어 감염력이 있는 생존 바이러스(감염성 바이러스) 음전율을 추가 분석했다"라고 말했습니다. 이번 2상은 국내 13개 대학병원에서 경증과 중등증 코로나19 환자 113명을 대상으로 피라맥스 투여군과 위약 투약군으로 나눠 진행했다. 투여 후 28일까지 바이러스 억제와 임상지표에 대한 효과를 관찰했다.
신풍제약은 RT-PCR(실시간 유전자증폭) 진단 검사를 했을 때 음성으로 전환되는 환자 비율(음전율)을 일차 평가변수로 잡았다. 그 결과 피라맥스 투여군 52명과 위약군 58명 간 차이가 없었다. 신풍제약 관계자는 "일차 평가변수에서 원하는 만큼의 목표치를 달성하지는 못했다"면서도 "다만 임상 2상에서 피라맥스의 가능성을 확인해 임상 3상을 진행할 계획"이라고 설명했다.
신풍제약은 RT-PCR 기반 음성 기준값의 경우 위양성(가짜 양성) 등의 문제가 있다고 보고 감염력이 있는 생존 바이러스(감염성 바이러스) 음전율을 추가 분석했다. 신풍제약에 따르면 28일째 입원이나 산소치료가 필요할 정도로 중증으로 악화하는 환자 비율은 피라맥스 투여군 52명 중 2명(3.8%), 대조군 58명 중 5명(8.6%)이었습니다. 이 결과 역시 환자의 수가 적어 유의하지는 않았습니다.

안전성 평가에서 예상하지 못한 중대한 부작용은 피라맥스 투여군과 대조군 모두 나타나지 않았습니다. 가장 흔한 부작용은 오심(13.5%), 소화불량(11.5%), 두통과 설사 등이었습니다. 신풍제약 관계자는 "임상 2 상의 목표치에 달성하지 못한 건 맞다"라면서도 "통계적 유의성을 확보하지 못한 지표에 대해서는 임상 3상 시험을 통해 확인할 것"이라고 말했습니다.
안전성 평가의 경우 위약군과 통계적 차이가 관찰되지 않았다. 가장 흔한 부작용은 오심(13.5%), 소화불량(11.5%), 두통과 설사 등이었다. 예상하지 못한 중대한 약물 이상반응(SUSAR)은 발생하지 않았다. 신풍제약 관계자는 "임상 2상에서 피라맥스 바이러스 억제 효과에 대한 근거와 전반적인 임상지표의 개선 가능성을 확인했다"며 "통계학적 유의성이 확보되지 못한 지표는 임상 3상 시험을 통해 최대한 신속히 확증하는데 전사 역량을 집중할 예정"이라고 말했다. 신풍제약은 이번 국내 2상 임상시험 결과를 바탕으로 이달까지 후속 임상 신청을 완료하고, 대규모 임상을 진행할 예정이다
'오늘의주식' 카테고리의 다른 글
| 오늘의주식 상한가종목 '범양건영' 상한요건 2가지 (0) | 2021.07.13 |
|---|---|
| 윤석열 탈원전 '서전기전' 관련주 (0) | 2021.07.06 |
| 오늘의주가 실시간 조회1위*카카오 (0) | 2021.06.15 |
| 오늘주가 실시간1위 *카카오 (카카오커머스 ,네이버쇼핑) (0) | 2021.06.14 |
| 대한민국 메타버스 사업(코인,대장주,게임) (0) | 2021.05.11 |




댓글